关于导致COVID-19的SARS-CoV-2的生物学和进化的入门和对话
关于导致Covid-19的冠状病毒SARS-CoV-2的文章有很多(至少是打字的)。然而,尽管它的故事占据了新闻周期,改变了我们所有人的生活,但很少有人谈论它的生物学,特别是它的进化。该病毒是快速进化的实时后果和动态的一个例子。它在中国重新进化,传播到另一个国家,改变了世界。它的力量远远大于它的体积,这种力量在进化生物学中更有意义。
为目前关于该病毒后果的讨论提供一些背景信息SARS-CoV-2,应用生态学教授罗伯•邓恩(RRD)坐下来汤姆·吉尔伯特(TG)来自进化全息基因组学中心,凯蒂Koelle(KK)来自埃默里大学,朱莉Casani(JC),马特Koci(可)大卫·拉斯穆森(DR)从NC州,和Sergios-Orestis Kolokotronis(SOK)从纽约州立大学来讨论病毒。或者更确切地说,他与他们坐在一起,虚拟地练习良好的身体距离练习。
下面的对话反映了参与者之间回应Rob问题的一系列电子邮件。感谢奥利维亚·桑切斯·邓恩帮助编辑文本的清晰度。
条款加粗和斜体字都包含在本文末尾的词汇表中。
最基本的
RRD:冠状病毒与其他病毒的区别是什么?
TG:非常哲学的问题,罗伯!但在最基本的情况下,有大约150个确定的病毒家族Cornaviridae都是这些家庭中的一员。定义为“包膜,积极意义单股基因组为的RNA病毒26 - 32个碱基长。”也就是说,它们有一层像信封一样的覆盖物。它们是以RNA为基础的DNA.它们虽然比细菌小,但比病毒大。直到最近最著名的Cornaviridae非典。*
科是病毒分类的一个关键单位,因为科是基于并定义了病毒的整体结构,例如,病毒的基因组基于什么(DNA、RNA、单链或双链等),基因组有多大,包含什么基因,病毒的外部是什么样子(包膜、蛋白质外壳)。来自其他家族的其他著名RNA病毒包括HIV病毒(在家族内部)Retroviridae)、甲型流感(家庭内)Orthomyxoviridae)、埃博拉病毒(在家庭内部)Mononegavirales)、麻疹(在家庭内副黏液病毒科)和普通感冒腺病毒(属内)Adenoviridae).
RRD:与最简单的细菌种类相比,冠状病毒有多大?哦,让我们用一个公共的单位集合。让我们用核苷酸(生命的遗传字母)来衡量大小,其中一个千碱基(kb)是1000个核苷酸。兆酶是一百万个核苷酸。
目前:SARS-CoV-2是导致2019冠状病毒病(Covid-19)的病毒,是一种+ssRNA病毒,大约有30个碱基(kb),所以是3万个核苷酸.这对RNA病毒来说是很大的。例如,流感病毒只有13.5个碱基,而艾滋病病毒的碱基少得可怜9.5个碱基。
TG:最小的细菌之一的基因组,尿道支原体相比之下,约有482个基因,长约580kb。一种细菌大肠杆菌有4000-5500个基因,基因组大小约4.6-5.3兆酶。
RRD:所以SARS-CoV-2的大小是3万个核苷酸,尿道支原体58万个核苷酸的大小和大肠杆菌大概有400万个核苷酸?这意味着从基因上来说,病毒要比病毒简单一百倍大肠杆菌.真是个流线型的小怪物。
* SARS影响了26个国家,2003年造成8000多例病例。
RRD:地球上有多少种病毒?有多少比例是未知的?
TG:呃……150 families I imagine the answer is enormous. If you assume each species has its own unique pool of viruses…and there are millions (hundreds of millions) of unique kinds of multicellular organisms that can be hosts…that is a very big number!
RRD:这还不包括攻击细菌的病毒,噬菌体,对吧?
TG:正确的。
RRD:什么是病毒?它是活的吗?
TG:这是一个复杂的问题。病毒的生存方式与细菌、植物或人类不同。病毒主要作为宿主内部的功能实体存在,宿主的细胞机制是病毒复制(复制其核酸,制造成为新病毒的新蛋白质等)所必需的。传统的生命形式——细菌、植物和人类——使用它们自己的细胞机制进行复制。
RRD:病毒也会利用宿主的细胞片段来隐藏自己。
TG:是的。
RRD:所以它们并不是完全活着,而是通过重新激活宿主身体的碎片来在世界上活动?这听起来很像……
TG:是的,我知道。僵尸。*
*病毒是否存活的不确定性甚至延伸到科学家和公共卫生官员谈论病毒的方式。例如,“活病毒”疫苗是指一种病毒仍然具有传染性,但被削弱了,从而能够触发人体的免疫反应,但不会引起疾病。换句话说,活病毒疫苗是由具有传染性的病毒制成的,但正如汤姆指出的,这些病毒从未完全活过。有时,我们甚至很难找到合适的词汇来描述远离我们可感知世界的生物世界。病毒就是这样。
起源与演变
RRD:关于这种导致Covid-19的SARS-CoV-2病毒的起源,我们知道些什么?它与哪种病毒最相似?根据什么?
TG:它与SARS的基因关系相当接近,已知的与病毒关系最密切的病毒是在蝙蝠身上发现的冠状病毒。蝙蝠是著名的病毒携带者病原体因为它们的免疫系统对病原体的反应不像人类那样强烈,所以被感染的蝙蝠通常没有强烈的症状(据我们所知)。关于这一现象的原因,有一些有趣的想法,与蝙蝠作为飞行动物所经历的大量细胞损伤有关。如果他们的身体对此反应过度,他们会自杀的。所以它们必须进化以降低对这种损害的反应,这也延伸到病原体。它们似乎能很好地应对充满病毒包袱的肚子。
蝙蝠冠状病毒是迄今为止发现的与SARS-CoV-2最接近的近亲,但这并不意味着它直接来自它们。它很可能从蝙蝠跳到中间宿主。穿山甲是一个很大的嫌疑。

RRD:什么可能会流入SARS-CoV-2如何能够在人与人之间传播?
克鲁舍:许多在人类体内循环的呼吸道病毒通过接触传播(两个人相互接触)、空气传播(我穿过你打喷嚏的空气)和环境传播(我接触你接触过的东西)的组合传播。如果一个人被打喷嚏或咳嗽后才会发生病毒传播,那么这种病毒的传播效率可能不如那些可以在门把手上停留2-3周的病毒。在门把手上,一个人可能在从未接近被感染者的情况下感染病毒。因此,这种冠状病毒通过这些不同的传播途径传播得如何,是影响其传播能力的一个重要因素。另一件对病毒传播能力有很大影响的事情是,当一个感染者出现症状时,这个人就会变得有传染性。如果一个人在知道自己生病之前就能传播病毒,那么这种病毒就有了很大的优势,疾病控制工作就会变得不那么有效。
RRD:在新闻中,我们听说该病毒有不同的“菌株”。这些新毒株自中国武汉病毒起源以来是否已经进化?我们怎么知道?
TG:很久以前(比如三天前),有人假设可能有两种“菌株”,S和l。S被假设为进入人类的原始菌株;L后来由S演变而来。但最近的分析发现,将这些菌株命名为“毒株”还为时过早。看起来像是两个菌株的只是一个菌株内部的变异,没有任何强烈的模式,无论是关于地理和历史.我们期待新的菌株进化,有些可能已经进化了,但缺乏数据来确定它们是否进化了,更不用说任何进化了或已经进化了的菌株是否具有新的特征,比如更容易传播的能力。
目前:一般来说,病毒会积累遗传突变随着它在人类中传播并扩大其地理范围。其中一些突变体在传播方面没有更好或更差,或者在传播方面更好,并与非突变体一起传播。其中那些更善于繁殖、生存和传播的物种在人类中的频率将会增加。
克鲁舍:这里需要补充的另一件事是:病毒中发生的一些突变不会改变病毒蛋白质的氨基酸,因此被认为对病毒的适应性(即它的传播潜力,或在个体之间传播的能力)没有很大影响。有些突变确实会改变病毒蛋白质的氨基酸,而且大多数情况下,这些突变是有害的。它们能降低病毒的传播能力。然而,一小部分突变是有益的。它们增加了病毒的传播潜力。
我们跟踪病毒循环模式通过观察所有这些类型的突变。通过观察哪些突变变得更常见,我们也可以开始更好地了解哪些突变可能是有益的,并可能使病毒更好地适应人类。这些突变是否真的有益应该通过实验来证实,因为其他因素(只是随机的机会,不同地理区域的环境因素等)也可能影响病毒种群中突变的常见程度的变化,特别是在流行病早期。
RRD:病毒还会以什么方式进化?
目前:变异菌株可能更能在人类之间传播,但它们也可能进化出传播给其他动物的能力。我们可以预测病毒的哪些部分可能与这种所谓的“主机切换”有关。病毒需要附着在宿主细胞上的受体上。对于SARS-CoV-2,我们知道一些遗传片段控制着病毒如何附着到宿主细胞的受体上并进入它们。这包括,例如,一种叫做”受体结合域一种叫做“刺突蛋白”的蛋白质(它与病毒外部的刺突有关)。正是这个基因片段产生了识别宿主细胞的蛋白质ptor血管紧张素转换酶2 (ACE2)因此,这一遗传段的基因对于了解病毒的起源非常重要。
RRD:换句话说,当病毒从有一种门的宿主切换到有另一种门的宿主时,我们期望与病毒敲开细胞门的方式相关的基因会进化?
目前:或多或少,是的。
TG:甲型流感就是一个典型的例子。禽流感“跳到”猪身上,在那里它适应了,并能够感染和在人类中传播,然后从猪传染给以猪为食的动物(例如丹麦的水貂)或靠近它们的动物(人类)。我不确定是否有从人类跳到猪的记录,但我假设是这样的。
RRD:这里暗含的意思是,猪门与人的关系比鸟门与人的关系更相似,所以能打开猪门的病毒更有可能打开人的大门。
TG:我们可能把这个比喻延伸得太远了,但是是的,你的受体和我的受体更像猪的受体而不是鸡的受体。
可:退一步说,我们主要担心来自动物的疾病开始感染人类,但我们也回馈。人流感传播给猪是相当普遍的.甚至有一些报告早在2009年,人们就把H1N1病毒传染给了他们的宠物狗和猫。芝加哥动物园的一只黑猩猩从人类那里感染了一种不同的呼吸道病毒(人类偏肺病毒)。这种情况发生的频率尚不清楚,因为我们并不经常去寻找它。
但我要补充的是,虽然这些病毒的突变帮助它们找到新的宿主来感染,我们也可以利用这些信息来建立治疗方法。病毒的某些部分起着非常重要的作用,如果蛋白质突变太多,或者在错误的位置,病毒就无法生长。当我们观察所有这些病毒的基因组时,我们可以看到这些区域,我们可以设计药物来对抗病毒的这些部分。所有的部分进化军备竞赛在我们和病原体之间。
H1N1,也被称为“猪流感”,是2009年流感大流行的罪魁祸首。

RRD:随着SARS-CoV-2的传播,它的毒性会增加还是减少?为什么?
TG:很难的问题。从进化的角度来看为了存活病毒需要最大化传播和存活如果死亡太快,就不会传播。然而,如果病毒进化到可以降低在个体中的复制速度,那么我们相互传播的肮脏物品(鼻涕、唾液等)中病毒的含量就会非常少,它就不会传播。“理想的”形式(从病毒的角度来看是理想的)可能就像普通感冒一样,它让你感觉有点糟糕,但还不足以让你躺在床上(从而避免别人)。它会让你打喷嚏、流口水,然后传染给别人。但它不会杀死你,让你继续打喷嚏,流口水和传播。注意,在这一点上,它可能已经是理想的……因为它不会杀死大多数人,当然也不会杀死最适合传播它的人(活跃的年轻人和孩子,他们比老年人和体弱者接触更多。所以如果它和现在有很大的不同,我会很惊讶。只是没有太多的选择来阻止它对老年人/体弱多病的致病性。
博士:SARS-CoV-2特别致命的原因之一是,它在肺部引起的炎症会导致类似肺炎的症状。这很大程度上是由我们自己的炎症反应引起的自我伤害。目前还不清楚引起这种类似肺炎的症状是否会对病毒有任何好处,甚至可能通过减少感染者的行动而降低其传播潜力。因此,病毒可能会有选择,从而在肺部引发侵略性较弱的免疫反应。但也有可能是,免疫反应更多地受宿主的控制,而不是病毒。这似乎确实是在老鼠身上的情况,在不同的老鼠品系中,它们对sars样冠状病毒的免疫反应存在巨大的遗传变异。
RRD:理想的病毒也会让它的宿主更喜欢社交,不太愿意强迫人们保持社交距离。
TG:继续说,如果它从人类身上跳到我们身边的另一个物种身上(很明显,它跳得相当远没有问题……即使它不是直接从蝙蝠身上跳到人类身上,而是通过一种中间媒介……),那么这也可能改变它的进化速度。可能会让它变多或变少,致命的/致病。无论是新的宿主物种,还是新的未来宿主物种,如果它跳回到人类身上。
RRD:我们还能预测它的进化吗?
TG:它肯定会继续分化成越来越多的菌株(或更准确地说,亚分支)。这是否有任何生物效应还有待观察,但人们可能会认为它会对……的功效产生影响疫苗并要求开发菌株特异性疫苗(有点像a型流感)
可:我同意Tom (TG)的观点,但我要补充一点,现在真的很难知道会发生什么,但我们的作为或不作为会影响它的演变。不是说疫苗不好,我们需要疫苗,但随着人口的增长免疫力这将给病毒带来新的进化压力。
RRD:哪种病毒基因进化最快?哪些基因需要进化才能让病毒在人类中成功传播(与蝙蝠或穿山甲相比)?
TG:我们需要和病毒学家或埃迪·霍姆斯这样的人谈谈,他正在研究迄今为止生成的序列,以得到一个好的答案!但可能是基因在最强选择下避开免疫系统或进入细胞,所以在病毒的外面。
可:作为病毒学家,我会说这将随着时间的推移而改变。在病毒第一次“跳跃”到人类并在人与人之间传播的早期,可能对许多不同的基因都有压力。与细胞结合的外表面基因,以及用来控制细胞的其他基因。既然它已经成功地在人类体内存在了一段时间,大多数进化压力将集中在刺突蛋白(再次强调,这是一种与病毒外部刺突蛋白相关的蛋白质,帮助病毒与宿主细胞结合)和其他与病毒膜相关的关键蛋白质上。然而,这种蛋白质的某些部分对于与宿主细胞的受体结合至关重要。所以进化很可能会以保存这部分蛋白质的方式发生,但仍然会以我们的免疫系统不再识别的方式改变其余的蛋白质。
Tom给Eddie发邮件。埃迪没有说哪种基因可能进化得最快,但他说,目前还没有证据表明毒性基因是进化得最快的。
RRD:如果大多数人都接种了疫苗(想象疫苗的存在和释放),病毒的进化或传播会有什么不同?
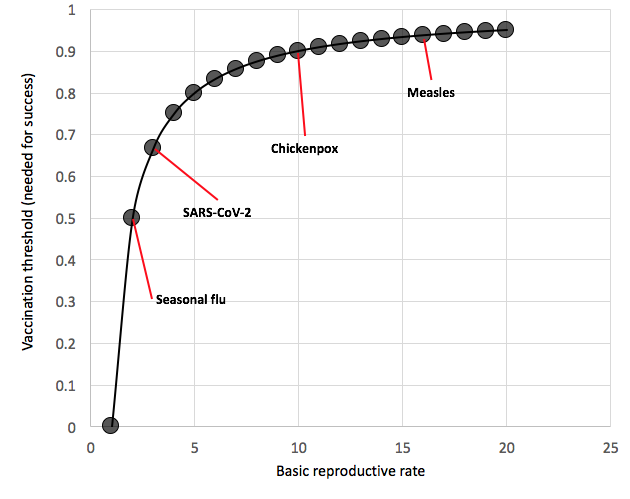
克鲁舍:接种疫苗对付这种病毒一般有两种可能的结果…如果接种率足够高,那么病毒将无法继续传播并灭绝。所需的疫苗接种水平称为疫苗接种阈值,它取决于传播潜力("基本复制编号, R0)的病毒。传播潜力越高,需要接种疫苗以阻止(甚至减缓)病毒传播的公众比例就越大。如果疫苗接种率仍然相对较高,但不足以阻止病毒传播,那么对一些人接种疫苗(前提是疫苗是一种高效、保护性的疫苗)实际上也会保护一些未接种疫苗的人。这被称为“群体免疫”,它的发生是因为接种疫苗减少了病毒传播的数量,因此降低了未接种疫苗的人也被感染的比率。
目前:我可以想象这种病毒在未接种疫苗的人群中传播,无论他们是病例还是无症状者。
克鲁舍:还有一种可能性是,高水平的疫苗接种(但低于疫苗接种阈值)可能会给病毒带来选择压力,使其逃脱疫苗提供的宿主免疫。在这种情况下,疫苗可能最终需要根据不同的病毒株重新配制。
博士:人类抗体针对冠状病毒的刺突结构域(图4中的红色三角形),病毒使用相同的蛋白质结合人类细胞受体,如ACE2(又是那些门)。这让病毒处于进化的困境中,因为如果它的刺突变化太多,它们就不能与宿主受体结合,但如果它们变化不够,它们就会被宿主免疫系统攻击。但这种困境并非冠状病毒所独有。例如,流感病毒的血凝素蛋白也可作为受体结合蛋白,同样也是人抗体的主要靶点。通过研究流感等病毒,我们知道这些蛋白质在耐受突变的能力上相当灵活,这使它们能够在保留其他生物功能的同时逃脱免疫系统。因此,尽管我的预测是推测的,但我认为SARS-Cov-2将能够逃脱由疫苗或自然免疫产生的人类抗体。事实上,有一些初步证据表明,HCoV-OC43等其他常见的人类冠状病毒会进化以逃避基于抗体的免疫。值得注意的是,这并没有降低开发疫苗的重要性,相反,疫苗可能需要随着时间的推移而更新,就像Katia (KK)上面提到的那样。
可这取决于给予何种豁免,以及豁免持续多长时间。有疫苗可以提供"消毒免疫“还有一些只是预防疾病。这些不同类型的保护以不同的方式驱动病毒进化。灭菌免疫是我们在大多数情况下所努力争取的,也是流感疫苗希望提供的免疫类型,当疫苗与流行菌株匹配时就会产生这种免疫。在这种情况下,在患者被感染之前,就已经诱导了他们体内高水平的抗体,然后当病毒出现时,抗体甚至会阻止病毒开始传播。这就是为什么每隔十年左右,你就会看到人类季节性流感病例中HA的主要亚型发生转变。当整个人群都有杀菌免疫(通过接种疫苗或感染)时,该亚型不再很好地循环,并被另一种亚型所取代。
如果你没有获得消毒免疫,你最终会受到一些低水平的感染(抗体会减缓,但不能阻止病毒在你体内传播),但这还不足以让你去看医生。这种亚临床感染允许病毒在人体中复制并获得新的突变,然后这只是一个达尔文选择的问题,直到一种传播更快或致死更快的病毒出现。在人类中有一些这样的例子,但研究得最好的例子是鸡的马立克氏病病毒疫苗。自从这种疫苗在20世纪50年代首次问世以来,每10-20年就会出现一种毒性更强的病毒,需要一种新的疫苗。
RRD:关于病毒的生物学我们应该注意什么?未知数是什么?
TG:它/它的菌株是否会发生突变,使其无效诊断测试?还是会影响疫苗的功效?
RRD:哦,天哪,我没有想过菌株可能会进化到无法检测的地步。
可:现在还为时尚早,但对我来说,最大的问题是对这些病毒的免疫力是怎样的。持续多长时间?我们每年都会看到几种冠状病毒。它们会引起普通感冒。每年我们都会被或多或少相同的病毒感染,因为我们对这些病毒的免疫力只能持续大约6个月。SARS-CoV-2也会这样吗?或者我们仍然会被SARS-CoV-2感染,但下次天气将会变冷。
RRD:什么是我没有问但我应该问的(如果你提出了这个问题,也要给出一些答案)?
TG:Covid-19是一回事,但这不会是唯一一次发生这种情况。我们如何阻止这种事再次发生?当政府行为不端时(例如压制真相、淡化影响、玩弄阴谋),我们又该如何处理这些略微尴尬的问题呢?说实话,我认为我们在Covid-19中已经非常幸运了,相比之下我们可能会结束。
JC:我认为我们需要考虑我们如何根据病毒的生物学特性调整我们的反应。在埃博拉之前,对州政府和当地居民的资助是按疾病分类的。我们非常努力地说,所有的应对措施在本质上都是相同的,只是疾病特有的细微差别,在很大程度上与传播的范围、规模和机制有关。每个回答都是建立在前一个回答的基础上的。幸运的是/不幸的是,爆发从来没有接近到足以测试我们所做的是否正确,很多时候我们不得不重新学习一些实践。此外,从来没有开发出强有力的研究方法来测试应对措施的组成部分,其中大部分来自“日常”小规模公共卫生实践或其他非卫生突发事件应对实践。
这意味着我们对结果进行了假设,并对H1N1病毒的发生感到惊讶孕妇的病死率特别高,老年人受到一定程度的保护。这与季节性流感非常不同,季节性流感是预测高危人群的模型。这一点直到大流行之后才意识到。随机对照试验等方法在紧急情况下不起作用,而包括定性分析在内的其他研究方法的适应性还没有得到充分尊重。
JC:也……对于Covid-19,如果能有研究/评估基础设施来评估隔离是有效的还是无效的,以及导致隔离有效的细微差别是什么,那就太好了。了解这一点可能使分层隔离更加有效,因为它在地理上传播。例如,武汉的社区隔离设法减缓了向外传播(注意,在这种情况下的隔离并不意味着消除传播,只是减弱传播,以便其他人可以做好准备,使卫生保健系统不至于不堪重负),但游轮隔离很可能对船上的人无效。一种方法不能适用于所有人。
RRD:是否有某种病毒(除冠状病毒外)的特殊能力或有关病毒的故事特别吸引你?
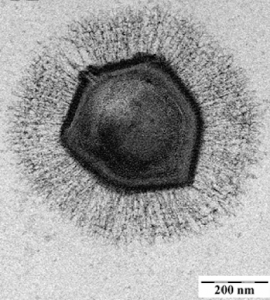
博士:我们往往会想到大多数病毒是高度适应于感染单一物种的专家。这些专家面临着权衡,限制了任何特定病毒株感染多个不同物种的能力。是什么
不幸的是,类似sars的冠状病毒等病毒实际上更像通才,可以在许多不同的宿主中繁殖。它们只需要一点时间来适应新的宿主。对我来说,这是一种鼓舞人心的东西,如此小和有限的基因组大小可以如此灵活。
TG:还有巨大的mimivirus,它引起了一些哲学上的头痛,关于病毒的定义是什么。通常它们的基因组大小和物理尺寸都和细菌一样大立克次氏体它们的基因组编码了通常在病毒中看不到的产物,包括核苷酸和氨基酸合成。但另一方面,它们没有蛋白质转译和能量代谢的机制,而这些是我们通常认为生物具有的特征。
目前:甲型流感病毒(抗原转移和漂移)。考拉逆转录酶病毒(既包括外生的,即个体间传播的,也包括内生的,即从父母遗传给后代的)。
JC:从预防的角度来看,我最喜欢的病原体是什么:一定是流感。这个小东西适应能力太强了,我们无法控制它,需要一种全新的方法。我们必须有现成的计划和不需要每年修改的疫苗。这些都与建立恢复力是一致的无论是生物的,社会的还是行为的:吸收创伤,为下一次做好准备。
TG:还有一些人类病毒一定来源于动物,但并不清楚是来自哪种动物。我认为,例如,天花仍然没有一个很好的动物起源的解释。还有野驴疱疹病毒.它的名字让我发笑。
可:病毒学家说,你还有多少时间?以上都有,但我最喜欢的话题之一可能是相对较新的领域水平基因转移通过病毒(从病毒到宿主,宿主到病毒),以及它们如何帮助植物和动物在进化中实现重大飞跃。举个例子,有证据表明逆转录病毒基因实际上为允许胎盘的发育.
我们是谁?
TG是汤姆·吉尔伯特的报道:汤姆在哥本哈根大学的全球研究所研究全息基因组学,即微生物和它们的宿主如何作为一个整体工作。
KK是Katia Koelle:卡蒂亚研究病毒的进化和传播,特别关注流感。她就职于埃默里大学。
David Rasmussen说:大卫开发了研究传染病流行病学和病毒进化的计算方法。他就职于北卡罗莱纳州立大学。
SOK是sergios - oretis Kolokotronis:Sergios研究传染病系统的分子进化和生态学。他在位于布鲁克林的纽约州立大学下州健康科学大学和位于纽约的美国自然历史博物馆工作。
罗伯·邓恩报道:罗伯研究与人类有关的物种的生物学。他在北卡罗莱纳州立大学应用生态系和哥本哈根大学进化全息基因组学中心工作。
JC是Julie Casani:朱莉有领导全州(美国马里兰州和北卡罗来纳州)应对突发公共卫生事件的经验。她在北卡罗来纳州立大学教授全球健康
Matt Koci报道:马特是一名病毒学家和免疫学家,研究鸟类宿主-微生物相互作用。他在北卡罗莱纳州立大学工作。
有用的链接
- 冠状病毒将如何终结?(如果你只读一样东西,就读这个).
- 将冠状病毒流行归咎于蝙蝠是错误的
- 坎贝尔博士的《根除疟疾,产生鸟粪的蝙蝠巢穴》
- 蝙蝠飞行和人畜共患病毒
- 冠状病毒生物学与流行病学
- 新型冠状病毒的成功
- 本周病毒学
术语表
用*表示的定义来自玛丽莲·鲁辛克的美丽的书,《病毒》,一本介绍101种不可思议微生物的插图指南附录是RRD为了清晰和上下文而添加的。。
抗体:防御蛋白由免疫系统产生,可以识别和中和病毒。
噬菌体(或简称为噬菌体):一种感染细菌的病毒,”这个词来源于拉丁语“吃”,但许多噬菌体杀死了它们的细菌宿主,但它们并不吃它们。“*
基本复制编号:在缺乏免疫力的人群中,由一个病例引起的预期感染人数。
诊断测试:识别和确认感染/病毒存在的医疗程序。
背景:脱氧核糖核酸,构成基因的物质(由核苷酸组成)。“*
信封:“一些病毒的外部部分,由从宿主细胞膜(偷来的脂肪)提取的脂质(脂肪)组成。“*
进化军备竞赛:两个相互竞争的有机体之间的一系列适应,使它们的生存机会比另一个更大。
基因突变:在翻译/转移遗传信息时发生的错误,这些遗传信息从那时起就被纳入了遗传密码中。这些突变对病毒可能是有害的,完全中性的,也可能是有益的。
水平基因转移:“基因从一个有机体到另一个有机体的运动。这通常是由病毒促成的(病毒在复制自己时,常常在宿主体内到处留下基因,就像心不在焉的教授有时会把钥匙甚至鞋子忘在身上一样)。“*
免疫:“宿主抵抗感染的能力。“*
核苷酸:“RNA和DNA的基本组成部分。“*
病原体:“引起疾病的微生物(大多数微生物不是病原体,大多数病原体也不会在人类中引起疾病。“*
阳性病毒RNA:可立即转化为宿主细胞并快速复制的遗传物质。
逆转录病毒:“一种病毒有一个RNA基因组,但它将RNA复制到DNA,并将DNA整合到宿主基因组中(郑重声明,这是一些非常狡猾的行为)。“*
消毒免疫:当宿主细胞含有抗体,阻止病毒进入,使其无菌。
Subclade:在生命进化树上的一个分支(枝)上,一个子分支,一个小枝。*
疫苗接种:“故意引入病毒以引起免疫反应。疫苗接种可以通过注射,也可以通过口服或鼻腔途径,可能涉及一种温和的病毒株、热杀死的病毒、病毒蛋白质或核酸。”接种疫苗有助于控制恶魔。接种标准疫苗。不幸的是,目前还没有针对导致Covid-19的病毒的疫苗。*
病毒传播模式:病毒在种群中传播和进化的速度。
毒性:“引起疾病的能力。”病毒的毒性越强,疾病的症状就越严重,出现最严重症状的感染者比例就越高。*
这篇文章是出版我在应用生态系学习。



